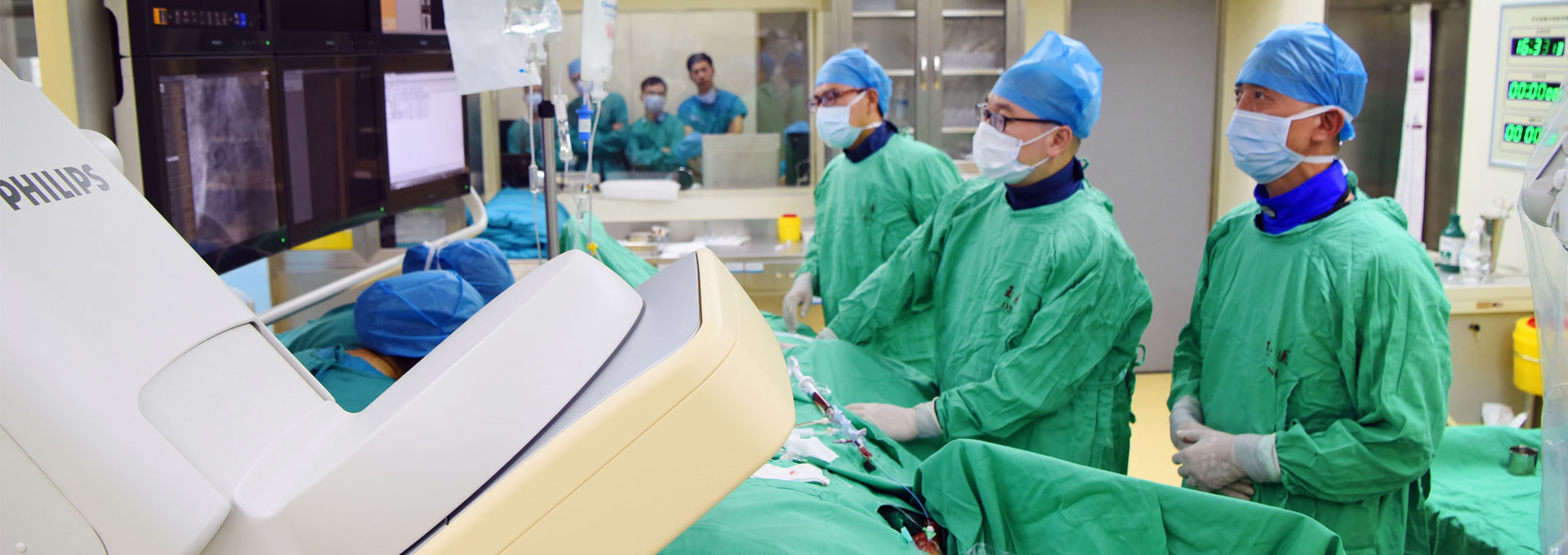
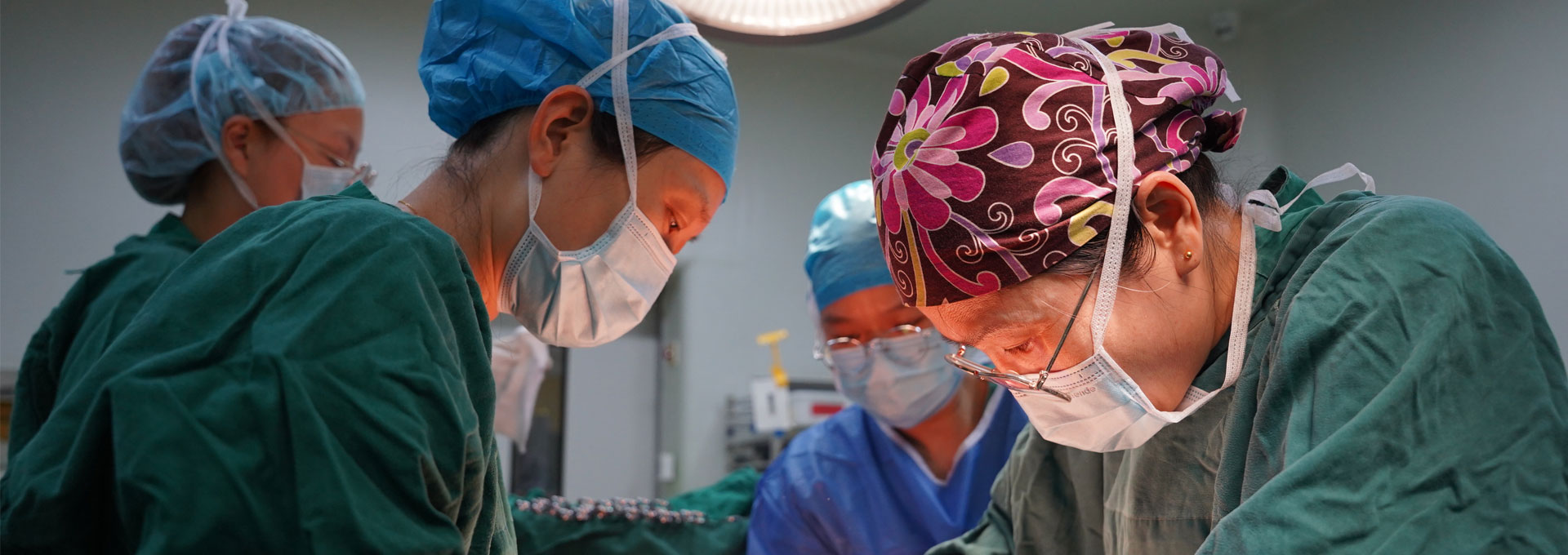
台州市市场监督管理局来院开展药物临床试验机构日常监督检查




为进一步规范药物临床试验过程,保障受试者权益与安全,提升临床研究质量,9月11-12日,台州市市场监督管理局组织检查组,对我院药物临床试验机构进行日常监督检查。我院党委委员、副院长陈孝敏及药物临床试验机构相关工作人员陪同。
检查组专家通过听取汇报、现场走访、资料查阅和人员问询等方式,对药物临床试验机构办公室、伦理委员会办公室、机构药房、机构档案室、伦理档案室、临床专业组等场所进行了全面细致的检查。
期间,专家们详细查看了药物临床试验管理制度、标准操作规程(SOP)及相关文档记录,并对机构人员、伦理委员及研究人员对药物临床试验相关法规和知识的掌握情况进行了现场询问。
同时,检查组重点抽查了呼吸内科专业组正在开展的临床研究项目《一项随机、双盲、多中心、事件驱动、平行对照、III期研究,评价PT027与PT007相比在有症状的中国成人哮喘患者中按需给药的有效性和安全性(BAIYUN)》。专家们对该项目的实施流程、文档管理、药物管理及伦理审查等方面进行了深入核查,并就试验中的关键环节与研究人员进行了交流。
在末次会议上,检查组对本次监督检查情况进行了总结,肯定了机构及专业组在药物临床试验管理中取得的成效,同时也指出了目前存在的问题与不足,并对机构、伦理委员会及专业组提出了具体的整改要求和建设性意见,希望以此为契机进一步优化管理体系,提升临床试验质量。
陈孝敏副院长表示,此次检查是对医院药物临床试验工作的一次全面检验,机构将认真对照检查组提出的问题和建议,逐项落实整改措施,不断完善药物临床试验管理制度和操作流程,切实保障临床试验的规范性、科学性和受试者安全。